Schwefelsäure und deren
Darstellung
| Eigenschaften: |
- hygroskopisch
- ätzend
-
reagiert mit Wasser
stark
sauer und unter starker Wärmeentwicklung |
| Verwendung: |
Herstellung von Düngemitteln, Waschmitteln
und Kunststoffe
|
| Strukturformel. |
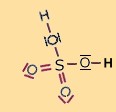 |
Schwefel steht in der 6.Hauptgruppe (3. Periode) und hat somit
6
Außenelektronen (Valenzelektronen). Gemäß der
Lewis Schreibweise verfügt es über 2 Elektronenpaare
sowie über 2 einzelne Valenzelektronen.
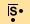
Da Schwefel in der
3. Periode steht, muss die Oktettregel, welche für die 2.
Periode verbindlich ist, bei Schwefel nicht eingehalten sein. In
dem Molekül Schwefelsäure ist der Schwefel von 10 Elektronen direkt
umgeben.
|
| |
Strukturformeln wichtiger Schwefel-Sauerstoffverbindungen:
|
|
|
|
Hydrogensulfat |
Hydrogensulfit |
Stickstoffmonoxid |
| |
|
|
|
|
|
Schwefeldioxid |
Schwefeldioxid |
Schwefeldioxid |
Schwefeldioxid:
farbloses, stechend riechendes Gas, nicht brennbar, entfärbt
organische Farbstoffe, Bleichung von Wolle und Stroh, wichtiges
Zwischenprodukt bei der Herstellung von Schwefelsäure. |
|
Doppelkontakt-
Verfahren: |
S+ O2
 SO2 SO2
2SO2+ O2  2
SO3 2
SO3
SO3+ H2O  H2SO4 H2SO4
|
|